PubMedで「イベルメクチン 癌治療」と検索すると300件以上の論文がヒットします。
その中の論文の一つをご紹介。
英語の論文ですが、Google Chromeなどでは日本語に変換できますので是非お読み下さい。
難しい方は太線や下線の部分だけ飛ばし読みして下さい。
次のブログで分かりやすく要約して解説します。
ーーーーーーーーーーーーーーーーー
イベルメクチンは冷たい腫瘍を熱い腫瘍に変換し、乳がんの治療において免疫チェックポイント阻害薬と相乗効果を発揮する
FDA承認の抗寄生虫薬であるイベルメクチンによる治療が、免疫原性癌細胞死(ICD)と乳がんへの強力なT細胞浸潤を誘導することを示す。
癌細胞と免疫細胞の両方で機能するATP/P2X4/P2X7軸のアロステリックモジュレーターであるイベルメクチンは、骨髄細胞やTreg細胞を含む免疫抑制細胞集団を選択的に標的とし、Teff/Treg細胞比の増強をもたらす。
いずれの薬剤も単独ではin vivoで有効性を示したが、イベルメクチンとチェックポイント阻害剤である抗PD1抗体との併用療法は、腫瘍増殖抑制において相乗効果を示し(p = 0.03)、完全奏効を促進し(p < 0.01)、さらに対側再発に対する免疫誘導をもたらし、抗腫瘍免疫応答が示された。
この併用療法は、原発性腫瘍のみならず、術前化学療法(p = 0.03)および術後化学療法(p < 0.001)後の再発率を有意に減少させ、転移性疾患においても治癒の可能性を示しました(p < 0.001)。
統計モデル化により、術後化学療法( p = 0.007)および転移性腫瘍(p < 0.001) の両方において、真の相乗効果が確認されました 。
イベルメクチンは乳がんにおいて免疫調節作用とICD誘導作用を二重に有し、低温腫瘍を高温腫瘍に変換するため、チェックポイント阻害薬と併用すると合理的に機序が明らかになります。
チェックポイント阻害薬は、患者自身の免疫システムを利用してがんを治療する画期的なアプローチとして登場しました。
しかし、チェックポイント阻害剤を単剤として使用した場合、一部の患者およびがん種にしか効果がありません。
最近の研究では、チェックポイント阻害薬の有効性は主に、すでに T 細胞が浸潤しているがん(いわゆる「ホット」腫瘍)に限定されることが示唆されています。
対照的に、「コールド」腫瘍では T 細胞浸潤がほとんどないか全くなく、一般的にチェックポイント阻害薬に反応しません。
乳がんにおけるチェックポイント阻害療法の臨床研究では、トリプルネガティブ乳がん(TNBC)に焦点が当てられています。
このサブタイプは変異負荷が高く、「免疫原性」が高いと考えられているためです。
ペンブロリズマブ(抗PD1抗体)単独療法の初期の第Ib相試験(KEYNOTE-012)では、進行TNBC患者の小さなサブセット(18.5%)で臨床活性の予備的な証拠が示されたが、第3相試験(KEYNOTE-119)では化学療法を超える改善は示されなかった。
単剤療法を超えて、チェックポイント阻害剤と化学療法の併用が研究されている。
アテゾリズマブ(抗PDL1抗体)とnab-パクリタキセルの併用は、IMpassion130でPD-L1陽性の切除不能な局所進行または転移性TNBCに有効であることが示され、2019年3月に乳がんに対する免疫チェックポイント療法として初めてFDAの承認につながった。
しかし、IMpassion131(アテゾリズマブ+パクリタキセル)は最近、陰性であると報告された。
そのため、チェックポイント阻害薬と相乗効果を発揮する乳がんのプライミング(「冷たい」腫瘍を「熱い」腫瘍に変える)が可能な薬剤を特定する必要性が高まっています。
最近報告された免疫原性細胞死(ICD)と呼ばれる現象は、宿主からの免疫反応を誘発する細胞死の一種です。
ICDは、アデノシン三リン酸(ATP)や高移動度グループボックス1タンパク質(HMGB1)の放出、カルレティキュリンの表面露出など、いくつかの特徴によって、古典的なアポトーシスやその他の非免疫原性または寛容原性の細胞死と区別されます。
癌患者において、ICDに基づく抗腫瘍免疫反応は、従来の化学療法剤による有益な結果と関連付けられています。
例えば、乳がんにおけるアントラサイクリンおよび大腸がんにおけるオキサリプラチンの有効性は、治療後の腫瘍内の細胞傷害性CD8 + Tリンパ球とFoxP3 +制御性T細胞の比率の増加と相関しています。
対照的に、固形がんにおける化学療法への反応不良は、リンパ球減少症と関連しています。
したがって、ICD誘導化学療法は、宿主の免疫系と連携して有効性を達成するようです。
しかし、化学療法は諸刃の剣です。
免疫細胞を刺激するだけでなく、抑制する可能性もあります。
免疫機能を抑制せずにがん細胞のICDを誘導する薬剤は、チェックポイント阻害剤との組み合わせに最適です。
FDA承認薬の中にそのような薬剤を探して、私たちのグループは、抗寄生虫薬イベルメクチンが乳がん細胞でICDを促進することを発見しました。
これまでの研究結果の中には、1975年以来世界中で使用されている抗寄生虫薬であるイベルメクチンがP2X4/P2X7プリン作動性経路を調節するというエビデンスがあり、イベルメクチンが腫瘍固有の高細胞外ATPレベルを抗がん活性にさらに活用する可能性を示唆しています。
注目すべきことに、P2Xプリン受容体4およびP2Xプリン受容体7(P2X4/P2X7)は様々な免疫サブグループに広く発現しており、イベルメクチンが直接的な免疫調節作用も有する可能性を示唆しています。
結果
イベルメクチンは「冷たい」乳がんを「熱い」腫瘍に変えることができる
我々はTNBCの4T1マウスモデルを用いて、イベルメクチンのin vivoでの効果を研究した。
HMGB1はすべての細胞に存在するクロマチンタンパク質であり、その放出はICD 21の特徴である。
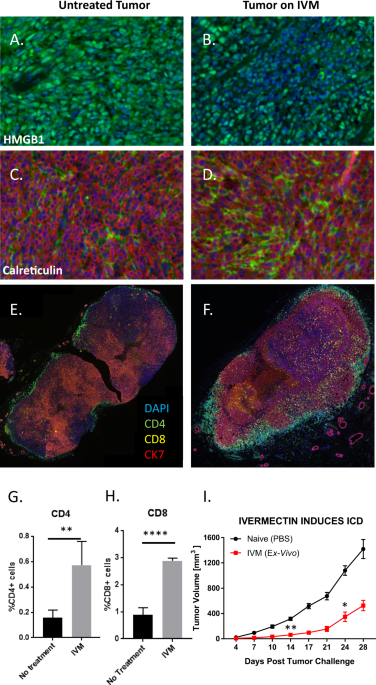
未治療マウスでは、腫瘍全体に均一にHMGB1染色(緑色)が観察された(図1A)。
対照的に、イベルメクチンで治療したマウスから単離した腫瘍では、HMGB1を欠くDAPI陽性細胞の大きな領域が見られ(図1B)、HMGB1が細胞外スペースに放出されたことを示唆している。
イベルメクチン治療はカルレティキュリン発現も変化させ、治療した動物の腫瘍ではカルレティキュリン発現の上昇(緑色)が観察され、このICD関連の貪食促進シグナルおよびメディエーターの有意な増加を示した(図1C、D)。
ERストレスを受けた細胞、損傷を受けた細胞、あるいは死にかけている細胞の表面にエンドソームカルレティキュリンを曝露すると、CD47に関連する「私を食べないで」シグナルとホスファチジルセリン(PS)曝露に関連する寛容原性の「私を食べて」シグナルの両方に拮抗することによって、免疫原性の貪食作用と抗原の交差提示が促進され、同時に貪食細胞上の受容体である低密度リポタンパク質受容体関連タンパク質(LRP)との相互作用が促進される。
イベルメクチンで治療した腫瘍ではCD4 + T細胞とCD8 + T細胞の強力な浸潤が認められたが(図1F)、未治療の腫瘍では認められなかった(図1E)。
イベルメクチンで治療した腫瘍では、未治療の腫瘍よりもCD4陽性(p < 0.01、図1G)およびCD8陽性(p < 0.0001、図1H)の細胞の割合が有意に高かった。
これらのデータを合わせると、イベルメクチンによる治療が 4T1 乳がんに ICD の特徴を誘発し、多数の CD4 +および CD8 + T 細胞をこれらの腫瘍に動員したことが示されています。
イベルメクチンが体内で ICD を誘発することをさらに確認するために、ICD 検出のゴールド スタンダードと考えられている古典的なワクチン接種法も使用しました。
つまり、4T1 細胞を IVM で処理して in vitro で ICD を誘発し、続いて未感作マウスに接種し、続いて生きた 4T1 細胞でチャレンジして腫瘍の成長防止を実証しました。
この実験では、生きた 4T1 細胞によるその後のチャレンジに対する防御が実証され、真のICD誘発の可能性が示されました( p < 0.01、図1I )。



イベルメクチンの直接的な免疫調節効果
イベルメクチンを体内で処理しても、処理した動物の脾臓から分離された様々なエフェクターおよび制御性 CD4(図S2A)または CD8(図S2B)T 細胞サブポピュレーションの頻度に有意な変化は見られませんでした。
しかし、コントロールマウスと 4T1 腫瘍を持つマウスから分離された脾臓細胞の機能的調査により、有意な免疫調節効果が明らかになりました。
接種後 1 ヵ月の腫瘍を持つマウスでは、CD11b +骨髄細胞集団の拡大を伴う脾臓が肥大し(図2A)、これには CD11b + GR-1 +骨髄由来抑制細胞(MDSC)と CD11b + GR-1 −単球/マクロファージ(Mon/Mac)の両方が含まれます。
イベルメクチンを体外処理すると、この拡大した CD11b +骨髄細胞集団が優先的に減少し、骨髄細胞と T 細胞区画のバランスが正常化しました(図2A)。
骨髄細胞集団とリンパ細胞集団は、イベルメクチンの用量増加に対して異なる感受性を示した(図2BおよびS2C)。
細胞タイプに合わせて調整した log 細胞数の線形混合効果モデルでは、CD11b +骨髄細胞がイベルメクチンに対して最も感受性が高いことが明らかになり、48 時間後に 4 μM、24 時間後に 8 μM、4 時間後に 16 μM という低濃度でも有意な減少を示し、この免疫抑制集団が迅速かつ選択的に標的とされていることが明らかになった(各結果、p < 0.0001)。
対照的に、CD4 または CD8 T細胞で同様の減少を達成するには、より高用量のイベルメクチンおよび/またはより長い曝露が必要であり、CD8 T細胞では 8 μM の 48 時間後または 16 μM の 24 時間後にのみ観察され、CD4 T細胞では最大曝露(16 μM の 48 時間)後にのみ観察された。
イベルメクチンが癌細胞と免疫細胞の両方で機能するATP/P2X4/P2X7シグナル伝達軸のアロステリックモジュレーターであることと一致して、骨髄細胞における感受性差はP2X7依存的であった(図2C )。
10μM KN62によるP2X7阻害は、イベルメクチンによるCD11b + GR-1 + MDSC、CD11b + GR-1 − Mon/Mac、およびその他の免疫サブセットの体外減少を回復させた( p < 0.001)。
より生理学的に関連する曝露条件を模倣するために、脾臓細胞を低用量の非細胞毒性イベルメクチンで処理したところ、曝露期間が長くなると、イベルメクチンはフィトヘマグルチニン(PHA)刺激T細胞に対して有意な増強効果を示し、CD8 +およびCD4 + Teff/Tregの比率を上昇させることが観察された(図2D) 。
PHAは、T細胞受容体(TCR)を含むがこれに限定されない糖鎖表面タンパク質に結合して非特異的なT細胞刺激を誘導し、TCRの架橋と下流シグナル伝達を引き起こし、T細胞の活性化と増殖をもたらす。
低用量の非細胞毒性イベルメクチンへの長期曝露による免疫増強効果は、TCR刺激(PHA経由)によって増強され、腫瘍担持マウスの脾細胞では阻害された(図2D)。
腫瘍担持マウスの脾細胞では、MDSCやPD-1を介した免疫抑制など、様々なメカニズムが適切なTCRシグナル伝達と機能を阻害することが知られている。



イベルメクチンは抗PD1抗体と相乗効果を発揮して腫瘍の増殖を抑制し、防御免疫を誘導する
イベルメクチンの抗癌ICD作用と直接的な免疫調節作用は、チェックポイント阻害薬との併用が可能である可能性を示唆した。
次に、イベルメクチンと抗PD1抗体を単独または併用した場合の有効性を、無治療と比較した(図S1Aの模式図)。
イベルメクチンと抗PD1抗体の併用により、無治療と比較して、経時的な平均腫瘍容積が有意に減少した(p < 0.001、図3A)。
縦断的腫瘍容積の結合統計モデルを用いたところ、イベルメクチンと抗PD1抗体は相乗効果を示し、これは薬剤の個々の効果の合計よりも有意に大きい効果と定義される(サブモデルp = 0.008、偽発見率/FDR 3%、表1)。
併用療法群では15匹中6匹、イベルメクチン単独群では20匹中1匹、抗PD1抗体単独群では10匹中1匹、無治療群では25匹中0匹で腫瘍の完全退縮が認められた。
イベルメクチンと抗PD1抗体の併用療法で腫瘍が消失したマウスに対し、対側乳腺脂肪層に10万個の4T1細胞を投与して再投与した。
これらのマウスは全て新たな腫瘍の発生を抑制した(図3B)。
一方、対照群では全てのマウスで腫瘍が発生した(データ未掲載)。
これは、イベルメクチンと抗PD1抗体の併用療法が、完全奏効例において防御的な抗腫瘍免疫を誘導することを示唆している。



併用療法の有効性のメカニズムをさらに理解するため、イベルメクチン、抗PD1、およびそれらの併用がT細胞の浸潤をどの程度増強するかを比較しました。
図3Cに視覚的に、また図3Dに定量的に示されたように、CD4 +およびCD8 + T細胞の4T1腫瘍への浸潤(21日目)は、イベルメクチンと抗PD1の併用療法後に最大でした。
抗腫瘍T細胞を測定するために、未治療、単剤治療、またはイベルメクチンと抗PD1の併用治療マウスから脾臓細胞を単離し、次に機能的T細胞応答のマーカーとしてCD107動員およびIFN-γ発現を測定するための標的として4T1細胞と共培養しました22。機能的な腫瘍特異的免疫応答は、イベルメクチンと抗PD1を投与したマウスでCD107およびIFN-γ陽性のCD8 + T細胞の個別の集団の存在によって確認されたが、抗PD1単独または未治療の対照を投与したマウスでは確認されなかった(p < 0.01; 図3E、F)。
臨床的に関連するあらゆる状況で効果的な併用療法
原発性腫瘍の制御を超えて、我々はこの併用免疫療法を主要な臨床的に関連する設定、すなわち術前補助療法、術後補助療法、および転移治療にわたって試験しようとした。
また、この併用免疫療法をインターロイキン-2 (IL-2)でさらに増強した場合の効果についても検討した。
IL-2は、T細胞活性化を誘導するために癌治療で効果的に使用された最初のサイトカインであった。
治療用抗腫瘍剤としてのIL-2の開発における主な課題は、IL-2がT細胞と制御性T細胞(Treg)の両方に作用できることである。
IL-2の対照的な作用は応答に一貫性がなく、癌免疫療法のための高用量IL-2の開発を制限していた。
IL-2の半減期を延長することは、IL-2ベースの免疫療法を改善するための有望な戦略であることが示されている。
これにより、治療活性に必要なIL-2の用量を大幅に減らすことができ、安全性と有効性の両方を高めることができる 。
我々は、半減期の延長した組み換えアルブミン-IL-2融合をイベルメクチンと抗PD-1療法(抗PD-1 + IL-2療法、簡略化して「IP」と呼ぶ)に追加することで、併用治療の有効性がさらに向上するという二次仮説を検討した。
術前補助療法は、がん治療においてますます重要な役割を果たすようになっている。
腫瘍接種後16日目に原発腫瘍を外科的に切除した後、術前補助併用療法を受けた動物の生存をモニタリングすることで、イベルメクチンと抗PD-1およびIL-2の併用療法を試験した(図S1Aの模式図)。
局所領域再発および遠隔転移の発生は生物発光イメージングによってモニタリングされ、ボディコンディションスコアの低下および病的兆候が認められた時点で動物は安楽死させられた。
未治療の動物はすべて、原発腫瘍の外科的切除後20~25日目頃に致死性疾患のために安楽死させられた(図4A)。
IP療法単独による治療では、約40%の動物が致死性疾患を発症せず、ある程度の生存利益が得られた。
最も良好な生存結果は、IP とイベルメクチン療法の併用で見られ、外科的切除後に約 75% の動物が長期生存者となった ( p < 0.05、図4A )。
生存している治療マウスは、反対側の乳腺脂肪層にある 4T1 細胞 100,000 個で再チャレンジされた。
IP 治療を受けたマウスの大部分は新しい腫瘍を発症せず、これは長期にわたる腫瘍特異的免疫の発症を示している (図4B )。
一方、IP 治療を受けたマウスとコントロールの未治療マウスはすべて腫瘍を発症した。
これらの動物の脾臓細胞は 4T1 細胞に対して反応性 (ELISPOT 経由) を示し、IVM + IP 治療を受けた動物における抗腫瘍 T 細胞応答の証拠を示した (図4C )。
これらの結果は、IVM + IP 併用治療が術前療法に有効であり、応答者において潜在的に強力な防御的抗腫瘍免疫を誘導することを示唆している。




乳癌の治療は依然として手術が第一選択であるが、再発は多く、術後高リスク患者には術後補助療法が必要となる。
我々は、術後補助免疫療法として、イベルメクチン、抗PD-1抗体、および組換えIL-2を単独または併用した場合の有効性を評価し、その有効性を検討した。
ルシフェラーゼを発現する4T1細胞(0.5 × 10 6、4T1-Luc)を雌BALB/cマウスの乳腺に注入し、10日間かけて触知可能な腫瘍へと増殖させた後、腫瘍を外科的に切除した。
術後補助療法を模倣するため、治療は術後2日目に開始された(図S1Aの模式図)。
再発および転移の発生は、生物発光イメージングにより複数の時点でモニタリングされ(17日目を示す、図4D)、その後、動物は、ボディコンディションスコアの低下および罹患の兆候に基づく安楽死基準を満たすまでモニタリングされた。
抗PD1またはIVM単独による治療では、未治療の対照と同様の生存率が得られました(図4E)。
イベルメクチンと抗PD1(IL-2の有無にかかわらず)の併用で治療した動物は、生存期間が有意に延長し、約40%の動物が長期生存者になりました(p < 0.001、図4E)。
統計モデル化により、イベルメクチンと抗PD1の併用は、IVMまたは抗PD-1単独と比較して非常に相乗効果があることがわかりました(サブモデルp = 0.007、FDR 2%、表2)。
興味深いことに、IL-2を追加しても、イベルメクチンと抗PD-1抗体の併用による生存率の利益はそれ以上向上しなかった(サブモデルp = 0.51、FDR 67%、表2)。
これらのデータは、イベルメクチンと抗PD-1抗体(IL-2の有無にかかわらず)による治療が、術後補助療法として有効であることを示しており、並行して行われた体重測定に基づく薬剤関連毒性や相乗毒性の証拠は得られなかった(図S1B)。
転移は、乳がんを含むがん患者の主な死亡原因です。
転移の状況でこの併用療法の有効性を試験するために、手術後の動物の少なくとも25%に検出可能な転移が見られるまで(通常、原発腫瘍の外科的切除後7日目)、治療を延期しました。
転移の進行は生物発光イメージングでモニタリングし(図S1Aの模式図)、動物はボディコンディションスコアの低下と罹患の兆候に基づいて安楽死基準を満たすまでモニタリングされました(例は図4Fに示す)。
未治療の動物はすべて、原発腫瘍の外科的切除後20~40日目頃に転移性疾患のために安楽死が必要となりました(図4G )。
IVM単独による治療では、未治療の対照と比較して、生存期間がわずかに延長しましたが、有意ではありませんでした(図4G)。
抗PD-1のみで治療した動物では生存期間がわずかに延長した(p < 0.05)が、IVM単独群と同様に、60日目までにすべての動物が安楽死を必要とした。
イベルメクチンと抗PD-1(p < 0.001)、またはイベルメクチン、抗PD-1、IL-2(p < 0.01)で治療した動物では、未治療の対照と比較して生存期間が有意に延長した(図4G)。
併用療法を受けた動物の約40%が長期生存者となる。
転移性の設定での生存に対するIVMと抗PD-1の併用効果は、IVMまたは抗PD-1単独と比較して非常に相乗的であることが再び判明した(サブモデルp < 0.001、FDR < 1%、表3)。
術後補助療法の場合と同様に、IL-2の追加はイベルメクチンと抗PD-1抗体の併用による生存率のさらなる向上を示さなかった(サブモデルp = 0.64、FDR 73%、表3)。
これらのデータは、イベルメクチンと抗PD-1抗体(IL-2の有無にかかわらず)による治療が転移性腫瘍においても有効であることを示しています。
議論
イベルメクチンは1970年代半ばの発見以来、世界中で7億人以上が河川盲目症やリンパ系フィラリア症の治療薬として安全に使用してきました。
安価で入手しやすいという利点もあります。
私たちの研究結果は、イベルメクチンによる治療がICD誘導を介して乳がんへの強力なT細胞浸潤を誘導し、「冷たい」腫瘍を「熱い」腫瘍に変化させることを示しています。
従来の化学療法薬とは異なり、この薬剤は宿主の免疫機能を抑制しないという利点があり、むしろ有益な免疫調節作用を有するため、免疫チェックポイント阻害の有望なメカニズム的パートナーとなっています。
高レベルの細胞外ATPの放出と蓄積は、腫瘍微小環境の重要な特徴であり、ICDの特徴として明らかになっています。
我々と他の研究者らは、イベルメクチンがプリン作動性シグナル伝達と、癌細胞と免疫細胞の両方で機能するATP/P2X4/P2X7/パネキシン-1軸の正のアロステリック調節因子であることをこれまでに示してきた 。
体外で処理したマウスの脾臓細胞において、イベルメクチンはP2X7依存的に様々な免疫サブポピュレーションを選択的に標的とすることができること(図2B、C)、そしてTreg細胞や骨髄細胞を含む免疫抑制集団に対する免疫エフェクター集団の比率の増加に関連する免疫増強活性を有することを明らかにした(図2A、D)。
イベルメクチンによる異なる免疫集団の選択的標的化は、マウスの脾臓Treg(CD4 + CD25 +)はCD8 +およびCD4 + CD25 − T細胞と比較して、増加する(> 100 μM)細胞外ATP投与量に対する感受性が高いことを示した以前の報告と一致している。
細胞外ATPに対するこの異なる感受性はP2X7依存性であり、表面P2X7受容体発現レベルと直接関連している(CD4 + CD25 + > CD4 + CD25 − > CD8 + T細胞)。
最近の報告では、ATP/P2X7軸はMDSCおよびMDSC媒介性免疫抑制においても機能することが示されている。
これは、イベルメクチンが腫瘍を有するマウスから体外単離された増殖した骨髄細胞をP2X7依存的に選択的に標的とすることができるという我々の知見と一致している。
MDSC のさまざまなサブセットと腫瘍関連マクロファージ/好中球 (TAM/TAN) のイベルメクチンに対する相対的な感受性を解明し、腫瘍微小環境内および全身におけるさまざまな骨髄サブセットに対するイベルメクチンの生体内効果を検証するには、さらなる研究が必要となるでしょう。
ATP/P2X7依存性細胞傷害性の差は、イベルメクチンのin vivoでの免疫調節効果に対する1つの可能な説明である可能性があるが、最近の報告では、CXCL12/CXCR4を介したT細胞の遊走および炎症駆動型リクルートメントにおけるATP放出とP2X4依存性シグナル伝達も示唆している。
T細胞の活性化、増殖および遊走におけるP2X4の役割は、特にCD4 T細胞で顕著であり、これは、イベルメクチンがex vivoで処理した脾臓細胞のCD4 + Teff/Treg比を増加させる(図2D )およびCD4 + T細胞による腫瘍内浸潤を増強する(図3D)のに特に強力であることを実証した我々のデータと一致している。
したがって、イベルメクチンを投与したマウスにおけるT細胞の腫瘍への浸潤は、抑制細胞の選択的枯渇とリクルートメント効果の組み合わせを反映しているのかもしれない。
PD-1はTCRシグナル伝達の負のフィードバック制御因子として機能するため、イベルメクチンと抗PD-1チェックポイント阻害薬の相乗作用が腫瘍微小環境へのT細胞浸潤を促進することは特に興味深い。
P2X4/P2X7依存性パネキシン1(PANX1)の開口とATP放出は、免疫シナプスにおけるTCR開始およびATP駆動によるATP放出のフィードフォワードループを提供することで、T細胞活性化において中心的な役割を果たす。
したがって、P2X4/P2X7/PANX1受容体のアロステリックモジュレーターとしてのイベルメクチンの、癌細胞と免疫細胞の両方で機能するプリン作動性シグナル伝達を調節する能力は、腫瘍微小環境および免疫学的状況におけるATPレベルの上昇、例えばケモカイン/TCRシグナル伝達およびケモカイン/TCR駆動によるATP放出の規模によって増強される可能性がある。
後者の可能性と一致して、イベルメクチンのTeff/Treg比に対する増強効果は、PHAを介したT細胞刺激下ではより強力かつ持続的であることが示されました(図2D)。
免疫原性癌細胞死の誘導、免疫細胞の分化制御、そしてATPに富む腫瘍微小環境の制御といったイベルメクチンの多面的な効果が、生体内で免疫チェックポイント阻害薬との相乗効果にどのように寄与するのかを解明するには、さらなる研究が必要です。
免疫チェックポイント阻害剤(ICI)は、がん患者のごく一部にのみ単剤として有効です。
現在、数百件の臨床試験で、ICIとFDA承認薬または試験段階の薬剤との様々な併用療法が検証されています。
こうした併用療法は主に、相乗効果のメカニズム的根拠がほとんどないか全くない状態で、相乗効果を示す薬剤の部分的な有効性に基づいて行われています。
重要な点として、最近の解析では、これまでに報告された試験データから、ICIが他の薬剤と相乗効果または相加効果を示す証拠は見つかっておらず、むしろ相乗毒性が観察される可能性があることが示されています。
私たちは、イベルメクチンが免疫チェックポイント阻害薬の合理的なメカニズム的パートナーであり、どちらの薬剤も単独で作用しない場合でも真の相乗効果を発揮することを示しました。
PD-1 阻害とイベルメクチンの相乗効果は、イベルメクチンが免疫原性の癌細胞死と腫瘍への T 細胞浸潤を促進し、その結果「コールド」腫瘍が「ホット」に変化する能力と機構的に関連している。
対照的に、同様の 4T1 モデルにおいて、ドキソルビシンなどの ICD を誘発することでも知られる確立された第一線標準治療化学療法剤と組み合わせた PD-1 阻害の治療効果の評価では、持続的な反応や腫瘍の完全な退縮は得られなかった。
ドキソルビシン単独では腫瘍への有意な T 細胞浸潤は誘発されず、PD-1 阻害との相乗効果も示されなかった。
ドキソルビシンが腫瘍を「ホット」に変化させることも、PD-1 阻害と効果的に相乗効果を及ぼすこともできなかったのは、直接的な免疫効果を反映していると考えられる。
患者で達成された血漿レベルに対応する濃度のドキソルビシンは、末梢血単核細胞(PBMC)に対して有意な細胞毒性を引き起こします(図S3)が、生理学的に関連するレベルのイベルメクチンでは有意な影響は見られませんでした。
本研究で実証されたように、イベルメクチンとPD-1チェックポイント阻害薬の併用は、多くの動物において原発腫瘍の完全退縮をもたらし、反応を示した動物では抗腫瘍免疫が保護的に発現しました。
さらに、この新たな併用療法は、臨床応用を想定した術前化学療法、術後化学療法、転移巣切除といった状況において有効であることを実証しました。
がんに対するイベルメクチンの新たな二重作用機序に基づき、イベルメクチンはFDA承認の他の抗腫瘍免疫(ICI)の抗腫瘍活性を増強する可能性もあります。
さらに、イベルメクチンは安価であるため、発展途上国のがん患者を含むすべての人々が利用することができます。
本研究で提示する前臨床結果は、イベルメクチンと抗PD-1抗体の併用療法が乳がん患者を対象とした臨床試験に値することを示唆しています。
方法
マウスと治療
雌の BALB/c マウスを Charles River Laboratories から 5~8 週齢で購入し、City of Hope の動物飼育施設で病原体フリーの条件下で飼育した。
すべての手順は City of Hope の動物実験委員会の承認の下で実施した。
マウスの右乳腺脂肪層に 4T1 乳がん細胞 100,000 個を接種し、割り当てられた治療計画を開始する前に触診して腫瘍の移植を確認した。
治療には以下が含まれていた。
5 mg/kg のイベルメクチン (Sigma Aldrich、ミズーリ州セントルイス) を 6 日間毎日経口投与。
10 mg/kg の抗 PD1 (BioXCell、ニューハンプシャー州ウェストレバノン) を週 1 回皮下投与。
1.5 mg/kg の MSA-IL2 を 50 µL の滅菌 PBS で週 1 回腹腔内注射イベルメクチンは45%の(2-ヒドロキシプロピル)-β-シクロデキストリン(Sigma Aldrich、332593-1KG)に溶解し、以前報告したように1日量の半分の10 mg/kgで使用した。
イベルメクチン投与量と投与頻度は、動物観察と体重測定に基づき、最大の効果と目に見える薬物関連毒性がないように最適化された。
腫瘍の成長はデジタルノギスで週2~3回、最大56日間測定した。
腫瘍の成長が長さまたは幅1.5 cmに達した時点でマウスを安楽死させた。
腫瘍体積は(長さ × 幅2 )/2として計算した。
転移実験は、メスのBALB/cマウスの乳腺にルシフェラーゼ発現4T1腫瘍細胞(4T1-Luc)0.5×10 6個を皮下注射し、接種後14日目に原発腫瘍を外科的に切除することによって行われた。
転移の成長をモニタリングするために、Lago X光学イメージングシステム(Spectral Instruments Imaging、アリゾナ州ツーソン)を用いて生体内生物発光イメージングを行った。
マウス1匹あたりの全腫瘍量は、生物発光イメージングにより毎週評価した。
動物のルシフェラーゼ値が600,000 photons/s/cm 2 /steradianを超えたときに原発腫瘍の再発を認識した。
この閾値が選択されたのは、再現性のある検出の下限値(510,000)をはるかに上回っていたことと、最適化実験において600,000が一貫して最低閾値であり、その後常に値が増加して最終的に死に至るためである。
体重減少により測定したところ、経口イベルメクチンと全身抗PD1およびIL-2の併用による治療後には有意な毒性は認められなかった(図S1)。
ーーーーーーーーーーーーーーーーー
免疫チェックポイント阻害薬単独よりも、またイベルメクチン単独よりも、組み合わせた方が効果があったということ。
イベルメクチンを併用した方が抗癌剤の効きが良くなる、だから少量投与ですむということは私自身が患者さんで経験しています。
「できる治療はありません」と言われた末期癌の患者さんを数名診ていますが、抗癌剤投与をされている患者さんもおられ、抗癌剤を否定することなく、副作用が出ない用量内で使用しQOLを改善できるなら、患者さんにとってもこんなに良い治療はありません。
しかも安価です。
抗癌剤は高いけどイベルメクチンは安い。
抗癌剤をやめてイベルメクチンではなく、抗癌剤に併用してイベルメクチンを使用する、そんな方法の提案をこの論文はしています。
次回、要点をまとめた記事を書きますね。
お知らせ
アーカイブ配信チケットで見放題です↓
患者さんのリクエストで復活させた
化粧品と発酵素するりの記事は
コチラ![]()
便通・腸を整えて美肌を目指す 元皮膚科・現役肛門科の女医が教えるキレイ術
2020年12月25日に出版し、おかげさまで9刷目となり累計発行部数が3万部を超えるベストセラーになりました![]()
オシリを洗っている全ての人に届けたい。
お読み頂けると幸いです。
そして2冊目も出版しました↓
手に取って頂けると幸いです![]()
公式LINEでも情報発信中
敏感肌の私でも
かぶれずに使えて
なおかつ
美容効果を実感できる![]()
自分のために作った
オリジナルコスメはコチラ↓
ドクターズコスメならではの技術がぎっしり詰まってます![]()